Damos início a partir de agora ao estudo de um dos instrumentos mais importantes no universo da Química – a tabela periódica dos elementos. Vamos deixar de lado toda a abordagem histórica que traduz a origem da tabela por fugir dos nossos propósitos. O que é relevante saber é que a tabela que utilizamos atualmente foi elaborada por Dmitry Mendeleev, químico russo. A distribuição dos elementos na tabela está em consonância com os estudos de Bohr e Rutherford no que diz respeito a distribuição eletrônica.
Tabela periódica atual:
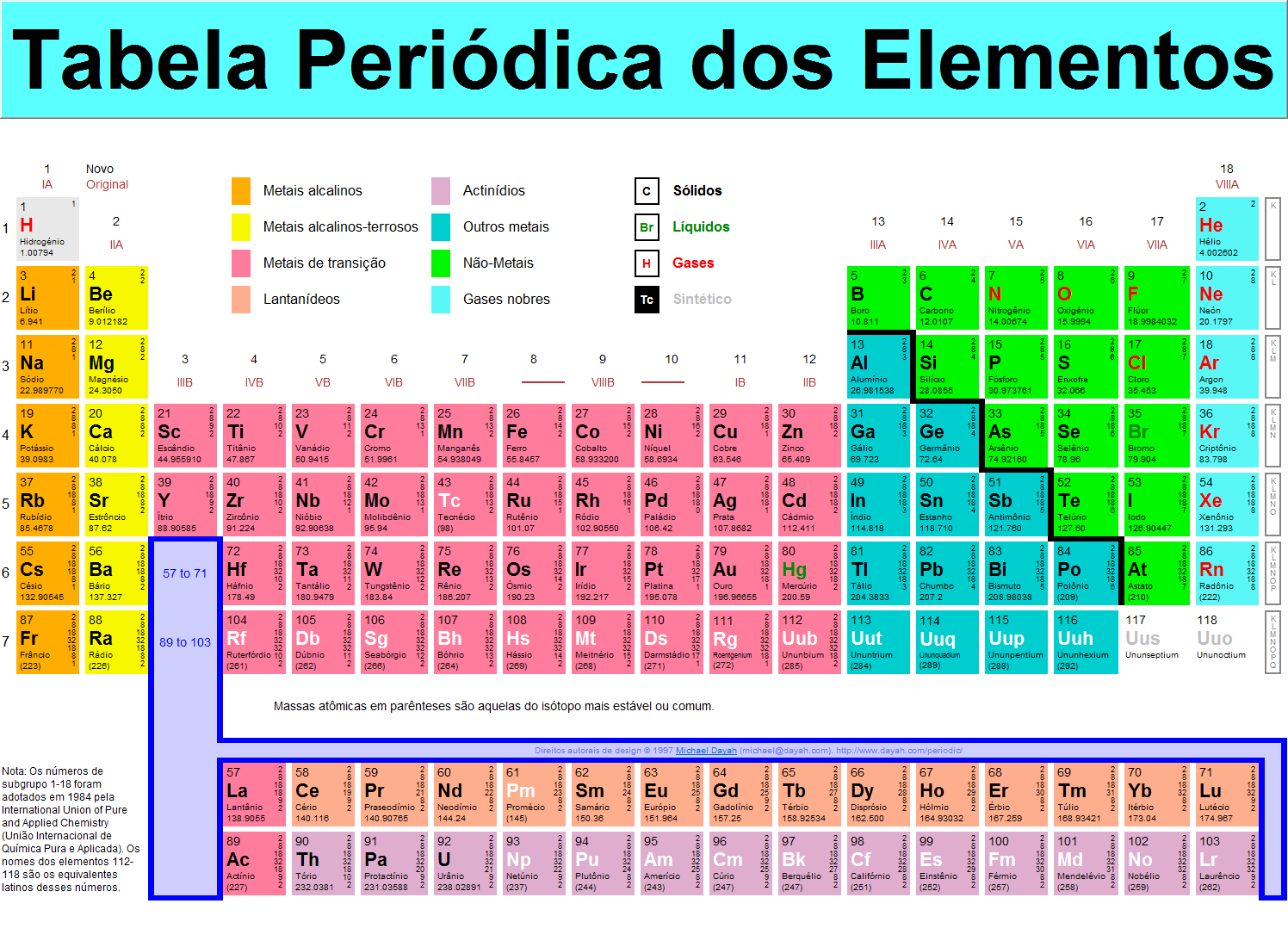
Os elementos na tabela estão dispostos em ordem crescente de número atômico, formando linhas chamadas de períodos, e colunas chamadas de famílias ou grupos. Atualmente são conhecidos 118 elementos químicos, contudo a IUPAC reconhece apenas 114 deles, estando em vias de reconhecimento dos outros.
Indice
Períodos
São as setes linhas da tabela e correspondem exatamente às sete camadas na distribuição eletrônica. Exemplo: se um elemento localiza-se no 5º período, significa que existem elétrons na sua quinta camada.
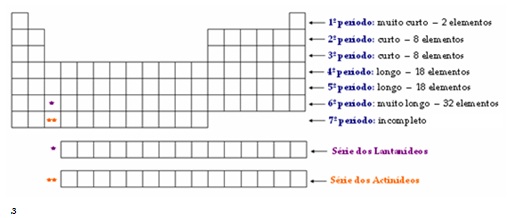
No 6º e 7º períodos há a série dos lantanídeos e dos actinídeos. Para facilitar a ilustração da tabela, eles são propositalmente colocados em séries destacadas. Caso isso não fosse feito, a tabela ficaria muito comprida e, por conseguinte, com difícil representação.
Grupos ou famílias
São as colunas da tabela periódica. É a classificação mais intimamente ligada às propriedades comuns dos elementos. Em alguns grupos, tais elementos possuem propriedades químicas muito parecidas. Antigamente, as colunas eram numeras por 1A, 2A, 3B, 4B etc. Atualmente, porém, são numerados simplesmente de 1 a 18. Além da numeração, as famílias podem ser chamadas pelo nome do primeiro elemento do grupo ou por nomes que já se popularizaram, a saber:
1 – metais alcalinos: Li, Na, K, Rb, Cs e Fr
2 – Metais alcalinoterrosos: Be, Mg, Ca, Sr, Ba e Ra
17 – Halogênios: F, Cl, Br, I, At
16 – Calcogênios: O, S, Se, Te, Po
18 – Gases Nobres: He, Ne, Ar, Kr, Xe e Rn
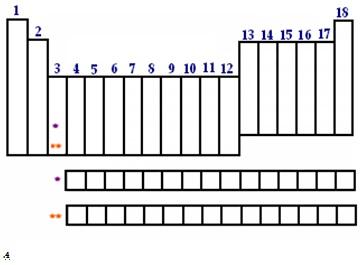
OBS: embora apareça no grupo 1, o Hidrogênio NÃO é um metal alcalino.
Blocos
Além das famílias e dos grupos, há também os blocos, outra divisão da tabela que leva em consideração os subníveis s, p, d e f dos elementos na distribuição eletrônica.
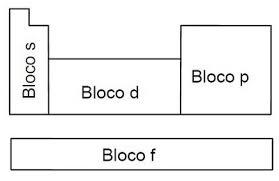
Os elementos são ainda classificados em metais, não metais, semimetais, gases nobres e há a colocação do Hidrogênio como autossuficiente em características, não sendo um metal.
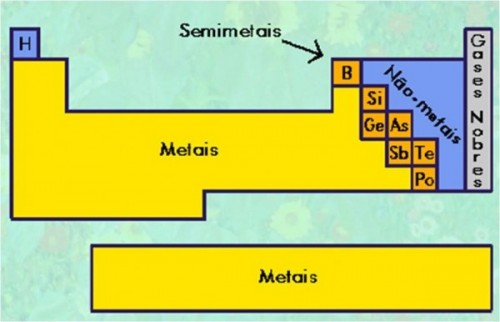
Concluímos aqui a análise da tabela periódica dos elementos. Compreendê-la é de suma importância para o estudo da Química e para facilitar o entendimento dos assuntos da disciplina. No próximo artigo falaremos das propriedades periódicas.
Até a próxima!


